MOVEMBER - Die häufigsten Fragen zu Prostatakrebs und ihre Antworten
Von Nicolas Platon, Radiologe, Affidea Schweiz
1. Tritt Prostatakrebs häufig auf?
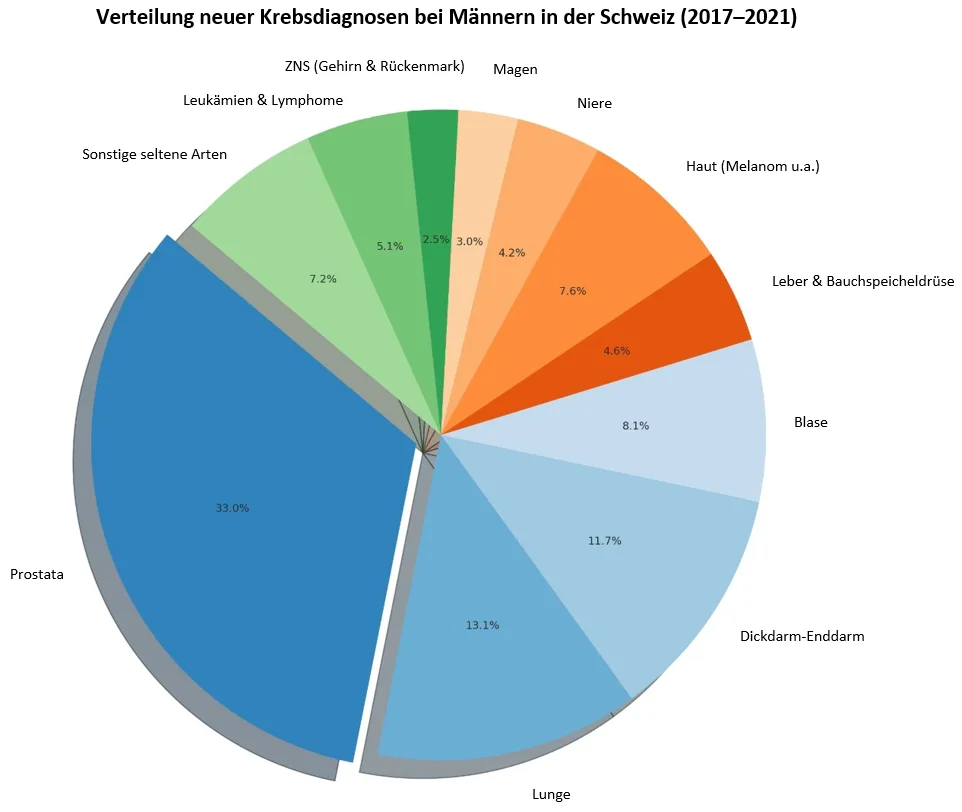
Ja. In der Schweiz ist Prostatakrebs die häufigste Krebsart bei Männern: Im Zeitraum von 2017 bis 2021 gab es pro Jahr im Durchschnitt 7 827 Neudiagnosen und 1 356 Todesfälle. Das Durchschnittsalter beträgt 70,7 Jahre bei der Diagnose und 83,1 Jahre zum Zeitpunkt des Todes. Vor dem 70. Lebensjahr liegt das Risiko einer positiven Diagnose bei etwa 7,5 %. Diese Zahlen spiegeln eine einfache Realität wider: Wir leben länger, wir erkennen Krankheiten besser und wir behandeln sie besser.
2. Gibt es organisierte Vorsorgeuntersuchungen in der Schweiz?
Nein, anders als bei Brustkrebs in einigen Schweizer Kantonen gibt es kein systematisches nationales Programm. Die Vorsorgeuntersuchung erfolgt individuell. Die Schweiz setzt auf Aufklärung und die gemeinsame Entscheidung von Patient und behandelndem Arzt oder behandelnder Ärztin.
Kurz:
Man bespricht den erwarteten Nutzen und die Risiken (falsch-positive Ergebnisse, Überdiagnosen) mit dem behandelnden Arzt und trifft dann gemeinsam eine Entscheidung.
3. Ab welchem Alter sollte man sich angesprochen fühlen?
Die Europäische Vereinigung für Urologie (EAU) plädiert für eine individuell angepasste Früherkennung und empfiehlt, Männern ab 50 Jahren den Test eines prostataspezifischen Antigens (PSA) anzubieten – bei familiärer Vorbelastung oder afrikanischer Abstammung ab 45 Jahren und bei BRCA-2-Mutation bereits ab 40 Jahren. Anschliessend wird das Testintervall an den ursprünglichen PSA-Wert angepasst.
4. Reicht der PSA-Test allein aus?
Das prostataspezifische Antigen (PSA) wird im Blut gemessen. Lange Zeit wurde der Test als Screening für Prostatakrebs beworben.
Das Problem dabei: Der Test ist einerseits zu empfindlich und andererseits nicht spezifisch genug. Konkret bedeutet das:
Ein erhöhter PSA-Wert kann auf Krebs hinweisen. Zu diesem Zeitpunkt handelt es sich aber lediglich um eine Warnung und nicht um ein Urteil.
Es kann auch einfach eine gutartige Vergrösserung oder eine Prostatitis, d. h. eine Entzündung der Prostata, vorliegen.
Umgekehrt können bei einem normalen PSA-Wert bestimmte signifikante Krebsformen unbemerkt bleiben.
In der Folge mussten sich viele Männer unnötigen Biopsien unterziehen und wurden manchmal sogar wegen einer Krebserkrankung behandelt, die niemals Probleme verursacht hätte (Überdiagnose, Überbehandlung).
Die Revolution: das MRT der Prostata

Seit etwa zehn Jahren wird vorrangig eine MRT-Untersuchung der Prostata angeboten. Die Biopsie wird nicht mehr automatisch unmittelbar nach einem ungewöhnlich hohen PSA-Wert durchgeführt.
Das MRT fungiert als selektiver Filter. Zeigt es einen verdächtigen Tumor, wird eine gezielte Biopsie durchgeführt, die vermieden werden kann, wenn das MRT unauffällig ist.
Gross angelegte Studien haben Folgendes ergeben: PRECISION (2018) hat gezeigt, dass das multiparametrische MRT vor der Biopsie dazu beiträgt, mehr aggressive Krebserkrankungen zu erkennen und unnötige Biopsien zu vermeiden. Vor kurzem hat STHLM3-MRI (2021) in gross angelegten Versuchen bestätigt, dass durch die Kombination von Blutbiomarkern und MRT die Anzahl der Biopsien und Überdiagnosen auf die Hälfte reduziert werden kann, während die Erkennungsquote signifikanter Krebsformen erhalten bleibt. Im Klartext: weniger invasive Untersuchungen, weniger falsch-positive Ergebnisse, mehr echte Krebsdiagnosen.“
Kurz:
PSA allein reicht nicht mehr aus.
Heute ist das Duo PSA + MRT der Schlüssel zu einer intelligenten Früherkennung.
Dies beruhigt viele Männer und ermöglicht es, Biopsien nur dort durchzuführen, wo sie wirklich notwendig sind.
5. Ist eine Biopsie mit Risiken verbunden?
Wenn der PSA-Wert oder das MRT einen Verdacht auf Krebs nahelegen, kann nur eine Biopsie Gewissheit bringen. Dabei wird unter örtlicher Betäubung ein kleines Stück der Prostata entnommen.
Bei der früheren transrektalen Methode wurde die Nadel unter Ultraschallkontrolle durch den Enddarm eingeführt. Dies hatte den Nachteil, dass die Rektalschleimhaut, die von Natur aus voller Bakterien ist, durchdrungen werden musste, was trotz vorbeugender Antibiotikagabe in 2 bis 5 % der Fälle zu einer Infektion (Sepsis), gelegentlich mit schwerem Verlauf, führen konnte.
Bei der neuen transperinealen Methode wird die Nadel durch die Haut des Perineums (Bereich zwischen Hodensack und Anus) eingeführt. Dies bietet folgende Vorteile: Vermeidung des Rektumdurchgangs und Senkung des Infektionsrisikos auf unter 1 % bei gleichzeitig höherer Präzision, insbesondere bei im MRT sichtbaren Tumoren. Diese Technik wird heute unter örtlicher Betäubung oder leichter Narkose ambulant durchgeführt.
Gezielte Biopsien dank MRT
Früher wurden Prostatabiopsien unter Ultraschallkontrolle durchgeführt, jedoch ohne Bild des Tumors: Man entnahm gemäss einem Raster systematisch 12 Proben, ohne zu wissen, ob man auf den Tumor stossen würde. Das nannte man „Blindbiopsien”.
Heute wird das MRT mit Ultraschall kombiniert (MRT-Fusionssonographie). Die Entnahme erfolgt gezielt im verdächtigen Bereich. Diese Methode ermöglicht es, unnötige Entnahmen zu vermeiden, signifikante Krebserkrankungen besser zu erkennen und die Überdiagnose kleiner, gutartiger Tumoren zu verringern.
Kurz:
Die Biopsie bleibt unverzichtbar, um eine Diagnose zu bestätigen. Dank der stark weiterentwickelten Technik birgt sie ein geringeres Infektionsrisiko (transperinealer Zugang) bei höherer Präzision (Führung durch MRT-Fusionssonographie).
6. Wird bei Feststellung einer Krebserkrankung automatisch operiert?
Nicht unbedingt. Bei Tumoren mit geringem Risiko ist eine aktive Überwachung die Regel: Wir beobachten den Verlauf genau mithilfe des PSA-Werts, des Prostata-MRTs und gegebenenfalls gezielter Biopsien, ohne sofort zu behandeln. Das Ziel ist es, die Lebensqualität zu erhalten, ohne dabei die onkologische Sicherheit zu gefährden.
7. Wenn eine Behandlung erforderlich ist: Nach welchen Kriterien wählt man Strahlentherapie oder Operation?
Lokalisierter Prostatakrebs mit mittlerem oder hohem Risiko kann auf zwei Arten wirksam behandelt werden:
Mit einem chirurgischen Eingriff: die totale Prostatektomie (heute zunehmend robotergestützt), bei der die Prostata und manchmal auch die benachbarten Lymphknoten entfernt werden.
Mit einer Strahlentherapie: heute sehr präzise (IMRT, VMAT oder sogar SBRT in wenigen gezielten Sitzungen), oft in Kombination mit einer vorübergehenden Hormontherapie.
Die Ergebnisse beider Methoden hinsichtlich der Krebsbekämpfung sind vergleichbar.
Der Unterschied liegt im allgemeinen Gesundheitszustand: Ein junger, gesunder Patient verträgt die Operation gut, während ein gebrechlicherer Patient oder ein Patient mit schweren Begleiterkrankungen oft zur Strahlentherapie überwiesen wird.
Zu den Nebenwirkungen der Operation gehört das Risiko von Inkontinenz und Erektionsstörungen. Bei einer Strahlentherapie können Harnwegs- oder Rektalreizungen sowie fortschreitende Erektionsstörungen auftreten.
Während manche den Krebs durch eine Operation „loswerden“ wollen, vermeiden andere lieber eine Operation und entscheiden sich für eine Strahlentherapie. Die endgültige Entscheidung wird immer durch das Tumorboard getroffen, das aus Urologen, Onkologen, Strahlentherapeuten und Radiologen besteht.
8. Was ist eine PET/CT-Untersuchung mit PSMA und für wen ist sie geeignet?
PSMA-PET/CT ist ein Bildgebungsverfahren der neuen Generation, das dank einer gezielten Injektion selbst kleinste Krebszellen in der Prostata sichtbar macht. Es wird vor allem bei Krebserkrankungen mit mittlerem oder hohem Risiko oder bei einem Rezidiv, wenn der PSA-Wert wieder ansteigt, empfohlen.
PSMA-PET/CT hat die Situation grundlegend verändert. Früher verwendete man CT-Scan und das Knochenszintigramm, um nach Metastasen zu suchen. PSMA-PET/CT ist sensitiver, da das Verfahren winzige Metastasen erkennt, die sonst manchmal unsichtbar bleiben, und spezifischer, da es echten Krebs besser von einem einfachen Artefakt unterscheiden kann. Im Jahr 2025 steht die Methode gemäss den europäischen Empfehlungen (EAU) nun im Mittelpunkt der Bilanz zum Auftreten signifikanter Prostatakrebserkrankungen.
9. Wie verändert sich die Strategie bei metastasierenden Formen?
Wenn sich der Krebs bereits ausgebreitet hat (Knochen-, Lymphknoten- oder Viszeralmetastasen), basiert die Strategie auf der Androgendeprivationstherapie (ADT).
Doch seit einigen Jahren wird die ADT allein als nicht mehr ausreichend betrachtet. Man spricht von einer frühzeitigen Intensivierung, und die Strategien lauten dann:
ADT + ein Antiandrogen der neuen Generation (ARPI)
ADT + Docetaxel: vor allem bei Erkrankungen mit starker Metastasierung
Gelegentlich ADT + ARPI + Docetaxel: Dreifachtherapie für bestimmte Profile
Kurz:
Die Gesamtüberlebenszeit wird um mehrere Jahre verlängert.
Das Fortschreiten der Erkrankung und Knochenkomplikationen werden verzögert.
Eine akzeptable Lebensqualität wird länger aufrechterhalten.
Heute begnügt man sich selbst im metastasierten Stadium nicht mehr damit, „das Testosteron auszuschalten“. Wir greifen von Anfang an hart durch, was die Prognose radikal verändert.
10. Welche neuen Therapien gibt es?
Der PSMA-Radioligand (Pluvicto® – Lutetium-177-PSMA-617) stellt einen bedeutenden Fortschritt bei fortgeschrittenen und resistenten Prostatakarzinomen dar.
Pluvicto® ist eine innovative Therapie, die sozusagen ein GPS-Gerät mit einer gezielten Bombe kombiniert. Das GPS ist der Ligand, der das PSMA erkennt, welches an der Oberfläche von Krebszellen vorkommt. Die Bombe besteht aus Lutetium-177, einem radioaktiven Isotop, das eine lokale Bestrahlung bewirkt. Der Radioligand zirkuliert, bindet sich an die Tumorzellen und zerstört diese von innen, wodurch Schäden am gesunden Gewebe begrenzt werden. Dies stellt einen bedeutenden Fortschritt für metastasierende, resistente Prostatakrebsarten dar.
In der Schweiz ist Pluvicto seit Februar 2023 für metastasierten kastrationsresistenten Prostatakrebs (mCRPC PSMA+) zugelassen, wenn eine Behandlung mit einem Antiandrogen der neuen Generation und einer Taxan-Chemotherapie versagt haben.
Die Wirkung besteht in einer Verbesserung der Gesamtüberlebensrate (VISION-Studie, NEJM 2021) und vor allem der Lebensqualität von Patienten, die bereits belastende Therapien durchgemacht haben.
„Bestimmte Formen von Prostatakrebs haben eine genetische Achillesferse: eine Mutation in den Genen BRCA1 oder BRCA2, dieselben, die auch bei bestimmten Brust- oder Eierstockkrebsarten auftreten.
Normalerweise helfen diese Gene der Zelle, ihre DNA-Fehler zu reparieren. Wenn sie defekt sind, wird die Zelle anfällig.
PARP-Inhibitoren, wie sie in der Kombination Akeega® (Niraparib + Abirateron) enthalten sind, nutzen diese Schwäche aus: Sie blockieren ein anderes System zur Reparatur der DNA. Ergebnis: Die Krebszelle kann ihre Schäden nicht mehr reparieren und stirbt schliesslich ab.
Das nennt man Präzisionsmedizin: Anstatt alle Patienten gleich zu behandeln, wird die Behandlung auf das genetische Profil des Tumors abgestimmt.“
Seit 2024 ist die Kombination Akeega (Niraparib + Abirateron + Prednison, mit ADT) in der Schweiz als Erstlinientherapie für mCRPC-Patienten mit einer BRCA1/2-Mutation zugelassen. Das Ergebnis ist eine deutlich verlängerte progressionsfreie Überlebenszeit und erstmals eine Behandlung, die wirklich auf das genetische Profil des Tumors abgestimmt ist.
Und morgen? Alpha-Emitter (225Ac-PSMA) befinden sich derzeit in klinischen Studien. Sie verwenden Actinium-225, das Alpha-Teilchen emittiert: Diese sind deutlich energiereicher als Beta-Strahlung (Lutetium), aber mit extrem kurzer Reichweite. Ihr Potenzial ist eine noch höhere Wirksamkeit, selbst bei resistenten Formen. Aktuelle Grenze: spezifische Toxizität (starke Mundtrockenheit aufgrund der Bindung an die Speicheldrüsen). Wir warten auf grosse randomisierte Studien, um ihren Stellenwert zu bestätigen.
Kurz:
Es gibt vielversprechende Fortschritte. Heutzutage wird Prostatakrebs „à la carte“ behandelt, je nach den biologischen und molekularen Merkmalen des einzelnen Patienten.
11. Was muss ich konkret im November tun?
Informieren Sie sich und bleiben Sie nicht passiv
Welche familiären Vorbelastungen gibt es? Sind Vater, Bruder oder Onkel betroffen?
Risikobehaftete Herkunft: Männer afrikanischer Abstammung und Träger der BRCA2-Mutation sollten früher zur Vorsorgeuntersuchung gehen.
Das Gespräch mit dem Arzt oder der Ärztin suchen
Ab einem Alter von 50 Jahren, beziehungsweise ab 45 Jahren bei erhöhtem Risiko, sollte die Frage eines „aufgeklärten” PSA-Tests angesprochen werden.
Durchführung eines MRT vor der Biopsie: Dadurch werden viele unnötige Behandlungen vermieden, und die Biopsien beschränken sich auf das, was wirklich zählt.
Auf eine gesunde Lebensweise achten
Gewicht: Übergewicht erhöht das Risiko für aggressive Krebserkrankungen.
Regelmässige körperliche Aktivität verringert das Risiko und verbessert die Überlebensrate.
Rauchen ist ein Risikofaktor für aggressivere Krebsarten und sollte vermieden werden.
Alkohol sollte in Massen genossen werden (indirekte Wirkung über Entzündungen und Stoffwechsel).
In der Praxis gilt: Was das Herz schützt, schützt auch die Prostata.
Nach einer Krebsdiagnose in Ruhe entscheiden, denn es gibt mehrere Strategien:
Aktive Überwachung bei wenig aggressiven Formen
Operation oder Strahlentherapie bei örtlich begrenzten Formen
Moderne systemische Therapien (hormonell, gezielt, Radioliganden) für fortgeschrittene Formen
Allein zu entscheiden, ist schwierig: Es ist immer eine Teamleistung von Patient, Familie und Spezialisten.
Die Schweizer Zahlen im Überblick
7 827 neue Fälle/Jahr (Durchschnitt 2017–2021)
1 356 Todesfälle/Jahr
Durchschnittsalter bei der Diagnose: 70,7 Jahre (zum Zeitpunkt des Todes: 83,1 Jahre)
Risiko vor dem 70. Lebensjahr: 7,52 % (Krebsdiagnose); 0,31 % (Tod)
Quelle: Krebsmonitoring Schweiz (BFS/NKS), Stand der Daten: 28.06.2024, veröffentlicht am 10.12.2024.
Was sich 2024/2025 wirklich verändert hat
Individuelle Vorsorgeuntersuchung (EAU): PSA-Test ab 50 Jahren, bei erhöhtem Risiko auch früher; nicht mehr, wenn die Lebenserwartung unter 15 Jahren liegt.
MRT der Prostata vor der Biopsie: bessere Erkennung der wichtigen Krebsarten, bessere Erkennung gutartiger Tumoren, weniger Biopsien.
Transperineale Biopsie wird empfohlen, um Infektionen zu begrenzen.
PSMA-PET/CT für das Staging bei mittlerem/hohem Risiko und bei Rezidiven.
mHSPC: systematische Intensivierung (ADT + ARPI ± Docetaxel ) – bestätigter Überlebensvorteil.
Schweiz: Pluvicto (177Lu-PSMA) zugelassen am 24.02.2023; Akeega (Niraparib + Abirateron) 2024 für mCRPC BRCA1/2 zugelassen.
Einfluss auf die medizinische Praxis
Was ändert sich in meiner täglichen Praxis? Die Qualität der Sortierung: Ein PSA-Test entscheidet nicht mehr über das Schicksal der Patienten: Das MRT verfeinert, die Biopsien zielen, die Biologie (Keimbahnmutation) gibt Orientierung, die PET-PSMA macht das Unsichtbare sichtbar, und die Therapien werden an das Patientenprofil angepasst. Unser Versprechen: Mehr Relevanz, weniger Überbehandlung.
Der Schnurrbart zieht die Blicke auf sich. Nutzen wir diese Gelegenheit, um die Aufmerksamkeit auf hochwertige Informationen und gemeinsame Entscheidungen zu lenken! Unser Ziel für 2025 sind nicht mehr Tests, sondern eine bessere Früherkennung.

Quellen (Auswahl)
Schweizer Zahlen: Bundesamt für Statistik – Krebsmonitoring Schweiz, Prostatakrebs (C61), 2017–2021 (veröffentlicht am 10.12.2024).
Schweizer Position zum organisierten Screening: Krebsliga Schweiz – Männer, informiert euch über Prostatakrebs! (10.11.2022).
Früherkennung (EAU 2024, Pocket): Empfehlungen für eine individuelle Vorsorgeuntersuchung, Alter und Risikofaktoren.
Leitlinien EAU 2025 (Aktualisierung): Moderne Staging-Verfahren (PSMA-PET/CT), mHSPC-Intensivierung, Biopsietechniken.
MRT vor der Biopsie: PRECISION, NEJM 2018; STHLM3-MRI, NEJM 2021 (+ Nachuntersuchungen 2024). PSMA-Radioligand (Schweiz): Swissmedic – Pluvicto/Pluvicto CA (Zulassung in der Schweiz am 24.02.2023).
In der Schweiz zugelassener PARP-Inhibitor-Kombinationswirkstoff: Janssen Switzerland – Akeega (Niraparib + Abirateron), Ankündigung vom 03.06.2024; compendium.ch (Liste A, Erstattung).
Alpha-Emitter in der Entwicklung: Zeitschriften 2024–2025 (Actinium-225-PSMA).
