Movember - Réponses aux questions les plus courantes sur le cancer de la prostate
Par Platon Nicolas, Radiologue, Affidea Suisse
1. Le cancer de la prostate est-il fréquent ?
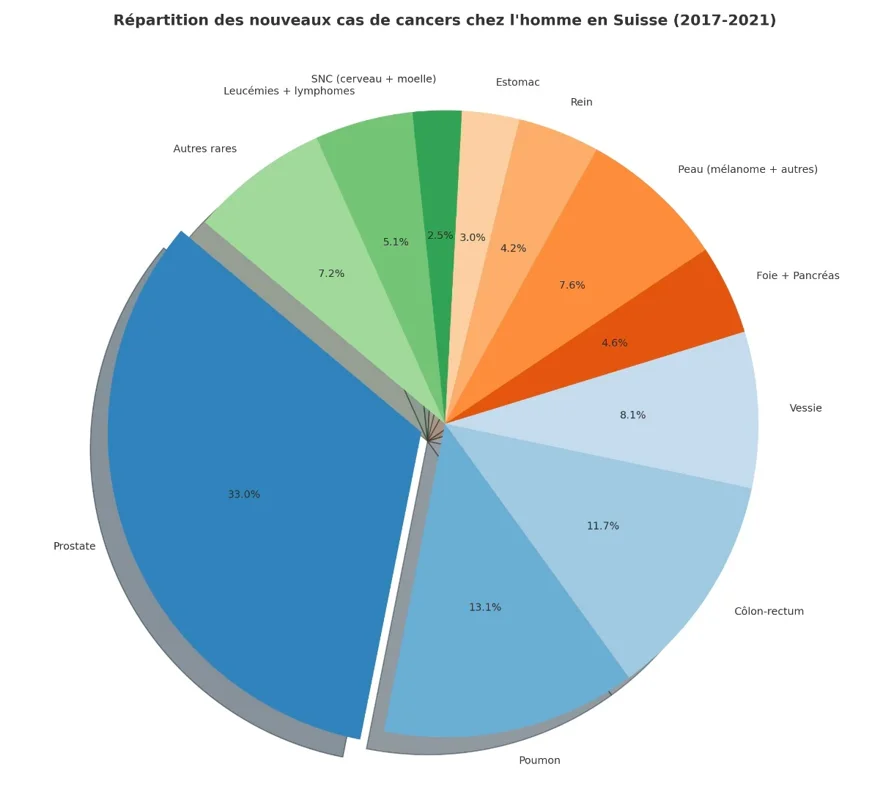
Oui. En Suisse, le cancer de la prostate est le cancer le plus fréquent chez l’homme : en moyenne 7’827 nouveaux cas par an et 1’356 décès sur la période de 2017 à 2021. L’âge médian au moment du diagnostic est de 70,7 ans et 83,1 ans lors du décès. Avant 70 ans, le risque d’être diagnostiqué est d’environ 7,5%. Ces chiffres résument une réalité simple : nous vivons plus vieux, nous dépistons mieux, et nous traitons mieux.
2. Y a-t-il un dépistage organisé en Suisse ?
Non, il n’y a pas de programme national systématique à l’inverse du cancer du sein pour certain Canton Suisse. Là, il s’agit d’un dépistage individuel. La Suisse privilégie l’information et la décision partagée entre le patient et son médecin traitant.
En résumé :
On discute du bénéfice attendu et des risques avec son médecin traitant (faux positifs, sur-diagnostic), puis on décide ensemble.
3. À quel âge faut-il s’y intéresser ?
Les recommandations européennes (EAU) plaident pour une détection précoce individualisée : proposer un antigène spécifique de la prostate (PSA) aux hommes informés dès 50 ans, plus tôt, dès 45 ans, en cas d’antécédents familiaux, d’ascendance africaine ou de mutation BRCA 2 dès 40 ans. On adapte ensuite la périodicité au PSA initial.
4. Le PSA seul est-il suffisant ?
L’antigène spécifique de la prostate (PSA) se dose dans le sang. Pendant longtemps, il a été présenté comme le test de dépistage du cancer de la prostate.
Le problème réside dans le fait qu’il est trop sensible mais pas assez spécifique. Concrètement :
un PSA élevé peut signaler un cancer. A ce stade, il s’agit alors d’une alerte et non d’un verdict ;
il peut aussi signaler une simple hypertrophie bénigne ou une prostatite, à savoir une inflammation de la prostate) ;
Inversement, avec un PSA normal, certains cancers significatifs peuvent passer inaperçus.
En résultat, beaucoup d’hommes se sont retrouvés avec des biopsies inutiles, parfois même avec un traitement pour un cancer qui n’aurait jamais posé problème (surdiagnostic, surtraitement)
IRM de la prostate: la révolution

Depuis une dizaine d’années, une IRM de la prostate est proposée en priorité. En effet, la biopsie n’est plus automatiquement effectuée directement après un PSA anormalement élevé.
L’IRM agit comme un filtre sélectif. Si elle montre une lésion suspecte, une biopsie ciblée est réalisée. Si elle est rassurante, elle peut être évitée.
Les grands essais l’ont démontré : « PRECISION (2018) a prouvé que l’IRM multiparamétrique avant biopsie permet de détecter plus de cancers agressifs et d’éviter les biopsies inutiles. Plus récemment, STHLM3-MRI (2021) a confirmé, à grande échelle, qu’en combinant biomarqueurs sanguins et IRM, on réduit de moitié le nombre de biopsies et le surdiagnostic, tout en maintenant la détection des cancers significatifs. En clair : moins d’examens invasifs, moins de faux positifs, plus de vrais cancers importants trouvés. »
En résumé :
Le PSA seul n’est plus suffisant
Aujourd’hui, le duo PSA + IRM est la clé d’un dépistage intelligent.
Cela permet de rassurer beaucoup d’hommes, et de focaliser les biopsies uniquement là où cela est vraiment nécessaire.
5. La biopsie est-elle risquée ?
Quand le PSA ou l’IRM fait suspecter un cancer, la seule façon d’être sûr est de réaliser une biopsie, à savoir prélever un petit fragment de prostate sous anesthésie locale.
Avec l’ancienne méthode, la voie transrectale, on passait l’aiguille par le rectum, guidée par une échographie. Cela représentait l’inconvénient majeur de traverser la muqueuse rectale, zone naturellement riche en bactéries, avec un risque d’infection parfois grave (septicémie) pouvant représenter jusqu’à 2 à 5 % des cas, malgré les antibiotiques préventifs.
Avec la nouvelle méthode, la voie transpérinéale, on passe l’aiguille par la peau du périnée (zone entre scrotum et anus). Elle offre les avantages suivants : éviter le passage par le rectum, diminuant ainsi le risque infectieux à moins de 1% et permettre plus de précision, surtout pour des lésions visibles à l’IRM. Cette technique s’effectue aujourd’hui sous anesthésie locale ou légère, en ambulatoire.
Des biopsies ciblées grâce à l’IRM
Avant, les biopsies prostatiques étaient réalisées sous échographie mais sans image du cancer : on effectuait 12 prélèvements répartis de façon systématique, comme un quadrillage, sans savoir si l’on tombait sur la lésion. C’est ce qu’on appelait des biopsies “à l’aveugle”.
Aujourd’hui, l’IRM est combinée avec l’échographie (imagerie de fusion IRM/écho). Le prévèvement s’effectue exactement dans la zone suspecte. Cette méthode permet de réduire les prélèvements inutiles, de mieux détecter les cancers significatifs, de diminuer le sur-diagnostic de petits cancers indolents.
En résumé :
La biopsie reste le passage obligé pour confirmer un diagnostic. Avec la technique qui a beaucoup évolué, elle offre moins de risques d’infection (voie transpérinéale), et plus de précision (guidage par imagerie de fusion IRM/écho).
6. Si un cancer est détecté, l’opération a-t-elle automatiquement lieu ?
Pas forcément. Pour les tumeurs à faible risque, la surveillance active est la règle : on suit de près grâce au PSA, à l’IRM prostatique, aux biopsies ciblées si besoin, sans traiter immédiatement. L’objectif est de préserver la qualité de vie sans perdre en sécurité oncologique.
7. En cas de nécessité de traitement, comment choisir entre radiothérapie et chirurgie ?
Le cancer de la prostate localisé, à risque intermédiaire ou élevé, peut être traité efficacement de deux manières :
Avec la chirurgie : la prostatectomie totale (de plus en plus robot-assistée aujourd’hui), qui consiste à retirer la prostate et parfois les ganglions voisins.
Avec la radiothérapie : aujourd’hui très précise (IMRT, VMAT, ou même SBRT en quelques séances ciblées), souvent associée à une hormonothérapie temporaire.
Les résultats des deux modalités en termes de contrôle du cancer sont comparables.
La différence se joue sur l’état de santé global : un patient jeune et en bonne santé tolère bien la chirurgie alors qu’un patient plus fragile ou avec comorbidités lourdes est souvent orienté vers la radiothérapie.
Les effets secondaires de la chirurgie sont un risque d’incontinence et de troubles de l’érection. Quant à la radiothérapie, ils peuvent présenter des irritations urinaires ou rectales et des troubles érectiles progressifs.
Alors que certains veulent « enlever » le cancer avec la chirurgie, d’autres préfèrent éviter l’opération et opter pour la radiothérapie. La décision finale est toujours prise en tumor board pluridisciplinaire, avec l’urologue, l’oncologue, le radiothérapeute et le radiologue.
8. Qu’est-ce que l’examen TEP/CT au PSMA et à qui s’adresse-t-il ?
Le PSMA-PET/CT est un examen d’imagerie de nouvelle génération qui, grâce à une injection ciblée, rend visibles même les plus petites cellules cancéreuses de la prostate. Il est surtout recommandé pour les cancers à risque intermédiaire ou élevé, ou en cas de rechute lorsque le PSA remonte.
Le PSMA-PET/CT a changé la donne. Avant, on utilisait le scanner + scintigraphie osseuse pour chercher les métastases. Le PSMA-PET/CT est plus sensible car il détecte des métastases minuscules, parfois invisibles autrement, et plus spécifique car il distingue mieux le vrai cancer d’un simple artefact. En 2025, les recommandations européennes (EAU) le placent désormais au centre du bilan d’extension des cancers prostatiques significatifs.
9. Comment la stratégie change-t-elle dans les formes métastatiques ?
Quand le cancer s’est déjà propagé (métastases osseuses, ganglionnaires, ou viscérales), la stratégie repose sur la thérapie de privation androgénique (ADT).
Mais depuis quelques années, l’ADT seule n’est plus suffisante. On parle d’intensification précoce et les stratégies sont alors :
ADT + un anti-androgène de nouvelle génération (ARPI)
ADT + docétaxel : surtout pour les maladies à fort volume métastatique
Parfois ADT + ARPI + docétaxel : trithérapie réservée à certains profils.
En résumé :
On prolonge la survie globale de plusieurs années.
On retarde la progression et les complications osseuses.
On maintient plus longtemps une qualité de vie acceptable.
Aujourd’hui, même au stade métastatique, on ne se contente plus « d’éteindre la testostérone ». On frappe fort dès le début, ce qui change radicalement le pronostic.
10. Quelles sont les nouvelles thérapies ?
Le Radioligand PSMA (Pluvicto® – Lutétium-177-PSMA-617) est une avancée majeure pour les cancers de la prostate avancés et résistants.
Le Pluvicto® est une thérapie innovante qui combine un GPS et une bombe ciblée. Le GPS, c’est le ligand qui reconnaît le PSMA, exprimé à la surface des cellules cancéreuses. La bombe, c’est le Lutétium-177, un isotope radioactif qui délivre une irradiation locale. Le radioligand circule, se fixe sur les cellules tumorales et les détruit de l’intérieur, en limitant les dommages sur les tissus sains. C’est aujourd’hui une avancée majeure pour les cancers de la prostate métastatiques résistants
En Suisse, depuis février 2023, Pluvicto est autorisé pour les cancers de la prostate métastatiques résistants à la castration (mCRPC PSMA+), après échec d’un anti-androgène de nouvelle génération et d’une chimiothérapie par taxane.
L’impact est l’amélioration de la survie globale (essai VISION, NEJM 2021) et surtout de la qualité de vie de patients déjà lourdement prétraités.
« Certains cancers de la prostate ont un talon d’Achille génétique : une mutation dans les gènes BRCA1 ou BRCA2, les mêmes que l’on connaît dans certains cancers du sein ou de l’ovaire.
Normalement, ces gènes aident la cellule à réparer ses erreurs d’ADN. Quand ils sont défectueux, la cellule devient fragile.
Les inhibiteurs de PARP, comme dans l’association Akeega® (niraparib + abiratérone), exploitent cette faiblesse : ils bloquent un autre système de réparation de l’ADN. Résultat : la cellule cancéreuse ne peut plus réparer ses dégâts et finit par mourir.
C’est ce qu’on appelle de la médecine de précision : au lieu de traiter tout le monde pareil, on cible le traitement en fonction du profil génétique de la tumeur. »
Depuis 2024, la combinaison Akeega (niraparib + abiratérone + prednisone, avec ADT) est approuvée en Suisse comme traitement de première ligne pour les mCRPC porteurs d’une mutation BRCA1/2. En résultat, la survie sans progression est nettement prolongée, et pour la première fois un traitement réellement adapté au profil génétique de la tumeur.
Et demain ? Les alpha-émetteurs (225Ac-PSMA) sont actuellement en essais cliniques. Ils utilisent de l’actinium-225 qui émet des particules alpha : beaucoup plus énergétiques que les bêta (lutétium), mais à portée ultracourte. Leur potentiel est lune efficacité encore supérieure, même dans les formes résistantes. Limite actuelle : toxicité spécifique (sécheresse buccale sévère liée à la fixation sur les glandes salivaires). On attend les grands essais randomisés pour confirmer leur place.
En résumé :
De nouvelles avancées prometteuses. Nous sommes entrés dans une ère où le cancer de la prostate se traite « à la carte », selon les caractéristiques biologiques et moléculaires de chaque patient.
11. Concrètement, que dois-je faire en ce mois de novembre ?
S’informer, ne pas subir
Connaître ses antécédents familiaux : père, frère, oncle atteint ?
Origine à risque : hommes d’ascendance africaine, porteurs de mutation BRCA2 : dépistage plus précoce.
Discuter avec son médecin
À partir de 50 ans (ou 45 ans si risque), aborder la question d’un PSA “éclairé”.
Réalisation d’une IRM avant biopsie : cela évite beaucoup de gestes inutiles et concentre les biopsies sur ce qui compte vraiment.
Soigner son hygiène de vie
Poids : l’obésité augmente le risque de cancer agressif.
Activité physique régulière : diminue le risque et améliore la survie.
Tabac : facteur de cancers plus agressifs, à éviter.
Alcool : modération (impact indirect via inflammation et métabolisme).
En pratique : ce qui protège votre cœur protège aussi votre prostate.
Si un cancer est détecté : prendre le temps, il existe plusieurs stratégies :
Surveillance active pour les formes peu agressives.
Chirurgie ou radiothérapie pour les formes localisées.
Thérapies systémiques modernes (hormonales, ciblées, radioligands) pour les formes avancées.
Décider seul est difficile : c’est toujours un travail d’équipe entre patient, famille et spécialistes.
Les chiffres suisses en bref
7 827 nouveaux cas/an (moyenne 2017–2021)
1 356 décès/an
Âge médian au diagnostic : 70,7 ans (au décès : 83,1 ans)
Risque avant 70 ans : 7,52 % d’être diagnostiqué ; 0,31 % de décéder
Source : Monitorage du cancer en Suisse (OFS/NKS), état des données au 28.06.2024, publié le 10.12.2024.
Ce qui a vraiment changé en 2024–2025
Dépistage individualisé (EAU) : PSA discuté dès 50 ans, plus tôt si risque ; on arrête si l’espérance de vie < 15 ans.
IRM prostatique avant biopsie : meilleure détection des cancers qui comptent, moins d’indolents, moins de biopsies.
Biopsie transpérinéale recommandée pour limiter les infections.
PSMA-PET/CT consacré pour le staging intermédiaire/élevé et la rechute.
mHSPC : intensification systématique (ADT + ARPI ± docétaxel) – bénéfice en survie confirmé.
Suisse : Pluvicto (177Lu-PSMA) autorisé (24.02.2023) ; Akeega (niraparib + abiratérone) approuvé en 2024 pour mCRPC BRCA1/2.
Influence sur la pratique médicale
Ce qui change dans ma pratique au quotidien ? La qualité du triage. Un PSA ne décide plus de votre destin : l’IRM affine, les biopsies ciblent, la biologie (mutation germinale) oriente, le TEP-PSMA révèle l’invisible, et les thérapies s’ajustent à votre profil. Notre promesse : plus de pertinence, moins de surtraitement.
La moustache attire les regards ; profitons-en pour attirer l’attention sur l’information de qualité et la décision partagée. En 2025, notre ambition n’est pas de dépister plus : c’est de dépister mieux.

Sources (sélection)
Chiffres suisses : Office fédéral de la statistique – Monitorage du cancer en Suisse, Cancer de la prostate (C61), 2017–2021 (publié 10.12.2024).
Position suisse sur le dépistage organisé : Ligue suisse contre le cancer, Messieurs, informez-vous… (10.11.2022).
Détection précoce (EAU 2024, Pocket) : recommandations pour un dépistage individualisé, âges et facteurs de risque.
Guidelines EAU 2025 (mise à jour) : staging moderne (PSMA-PET/CT), intensification mHSPC, techniques de biopsie.
IRM avant biopsie : PRECISION, NEJM 2018 ; STHLM3-MRI, NEJM 2021 (+ suivis 2024). Radioligand PSMA (Suisse) : Swissmedic – Pluvicto/Pluvicto CA (autorisation en Suisse le 24.02.2023).
PARP-inhibiteur combiné approuvé en Suisse : Janssen Switzerland – Akeega (niraparib + abiratérone), annonce 03.06.2024 ; compendium.ch (liste A, remboursement).
Alpha-émetteurs en développement : revues 2024–2025 (actinium-225-PSMA).
